Forschung
Bluttropfen kann Leben retten: Babyscreening auf Krankheiten
Mit einem Genomischen Neugeborenen-Screening könnten Babys auf Hunderte Krankheiten getestet werden. Forscher in Heidelberg und Mannheim arbeiten an einem flächendeckenden Konzept.
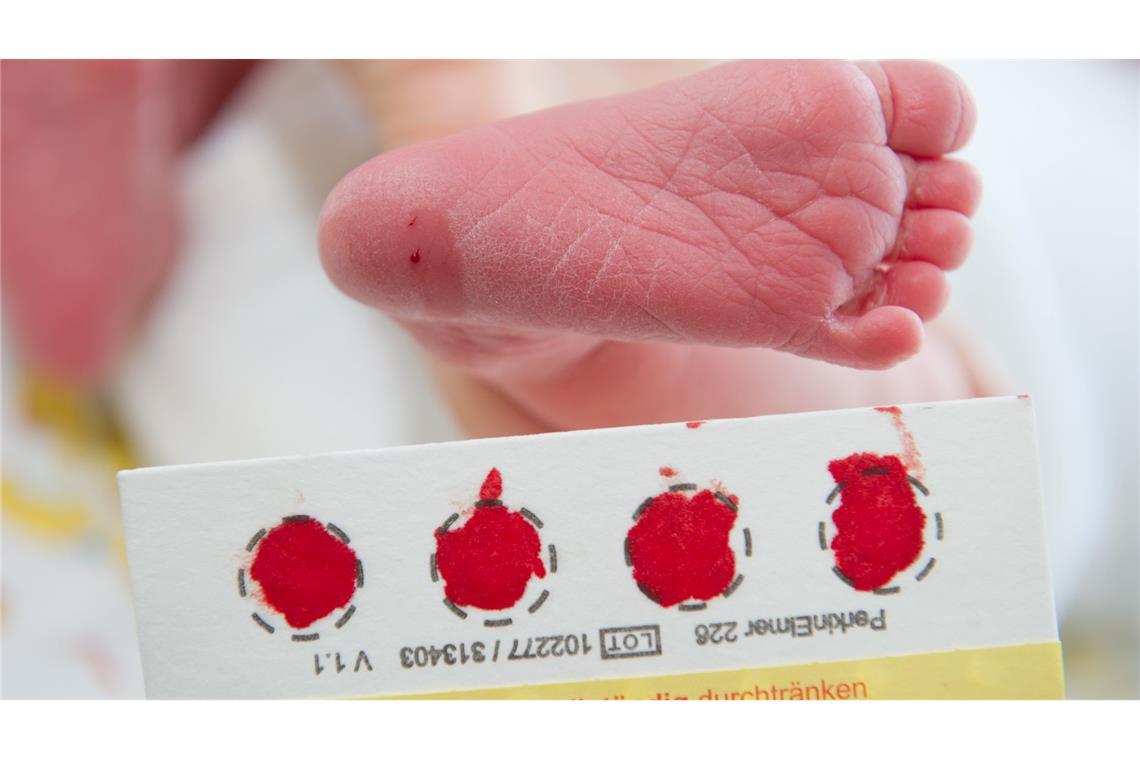
© picture alliance / Stefan Sauer/dpa-Zentralbild/dpa
Ein Bluttropfen vom Fuß eines Babys genügt, um viele Krankheit zu erkennen. (Archivbild)
Von Von Stefanie Järkel, dpa
Heidelberg/Mannheim - Es sind nur ein Pieks in den Fuß eines Babys und ein paar Tropfen Blut auf einer Pappkarte - doch mit dem Neugeborenen-Screening werden seit Ende der 1960er Jahre Leben gerettet und Lebensqualität geschaffen. "Das Neugeborenen-Screening ist laut Studien die erfolgreichste Maßnahme, um die Veranlagung für Krankheiten zu erkennen und dadurch Krankheitsverläufe positiv zu beeinflussen", sagt Christian Schaaf, Direktor des Instituts für Humangenetik am Universitätsklinikum Heidelberg.
19 Krankheiten werden damit erfasst, vor allem Stoffwechselerkrankungen. Doch dank der Entzifferung des menschlichen Genoms könnten mit einem Genomischen Neugeborenen-Screening Babys künftig auch auf Hunderte Krankheiten getestet werden.
Die Frage ist, wie viel wollen Eltern wissen? Soll auch auf Krankheiten getestet werden, die erst im Erwachsenenalter ausbrechen? Oder auf solche, die sich nicht behandeln lassen? Und wie lassen sich solch sensible Daten sicher speichern?
Forschungsprojekt New Lives erarbeitet flächendeckendes Konzept
In dem Forschungsprojekt New Lives erarbeiten Wissenschaftler am Universitätsklinikum Heidelberg sowie an den Universitäten Heidelberg und Mannheim noch bis zum kommenden Sommer ein flächendeckendes Konzept - und planen, von 2026 an in Heidelberg als Teil einer Studie mit einem Angebot des neuen Screenings zu starten. Die Finanzierung dazu ist beantragt. Allen Eltern von im Schnitt rund 3.000 Neugeborenen an der Uniklinik pro Jahr könnte dann ein Genomisches Neugeborenen-Screening angeboten werden, wie Schaaf sagt. Für das Screening wären demnach ebenfalls nur wenige Tropfen Blut notwendig. Die Ergebnisse sollten innerhalb von weniger als vier Wochen vorliegen.
Manuela Stecher wurde kurz nach Einführung des Neugeborenen-Screenings geboren - am 8. Mai 1969 in Pfullendorf, einer Kleinstadt nördlich des Bodensees. "Ich verdanke dem Neugeborenen-Screening alles", sagt die Diplom-Betriebswirtin, die kurz nach der Geburt positiv auf Phenylketonurie, einer schweren Stoffwechselerkrankung, getestet wurde. Dank des Screenings kann die Mutter zweier Kinder ein normales Leben führen, wie sie selbst sagt. "Ich würde jetzt nicht hier so dastehen. Ich wäre schwerst geistig behindert und hätte nicht dieses Leben."
Direkt nach der Diagnose begann für sie eine sehr strenge Diät, die sie ihr Leben lang einhalten muss. Dabei kann sie nur minimale Mengen an Eiweiß essen und braucht spezielle Nahrungsmittel, wie sie erzählt.
Bei einem von etwa 900 Kindern wird eine der seltenen Erkrankungen entdeckt
Aktuell wird laut Nationalem Screeningreport mit dem Neugeborenen-Screening bei einem von rund 900 Kindern eine der getesteten 19 seltenen Krankheiten entdeckt - also etwa bei 0,1 Prozent. Als Teil einer amerikanischen Studie wurden mit dem Genomischen Neugeborenen-Screening bei drei Prozent der getesteten Babys ernsthafte gesundheitliche Probleme entdeckt.
Die Heidelberger Forscher sprechen sich bei ihrem Konzept allerdings zunächst für eine striktere Auswahl der zu testenden genetischen Erkrankungen aus, wie Schaaf erklärt: Es sollte unter anderem nur auf Krankheiten getestet werden, die ganz sicher und noch im Kindesalter ausbrechen sowie auf Krankheiten, die sich behandeln ließen. Der Wissenschaftler geht davon aus, dass zunächst auf etwa 200 Krankheiten getestet werden könnte - und dabei vermutlich weniger als ein Prozent der getesteten Babys auffällig wären.
Beim Genomischen Neugeborenen-Screening würde laut Schaaf das gesamte menschliche Genom ausgelesen. Anschließend werde mit Filtern gezielt auf genetische Veränderungen geschaut, die für die ausgewählten Krankheiten verantwortlich seien. "Theoretisch sind diese genetischen Daten natürlich wie ein Fingerabdruck", sagt der Wissenschaftler.
Fundierte Beratung der Eltern entscheidend für Akzeptanz des Screenings
Die Heidelberger Uniklinik sei in der Lage, die Daten sicher zu speichern, sagt Eva Winkler, Verbundsprecherin von New Lives. Als Teil ihres Konzepts würden auch nur die genetischen Veränderungen gespeichert - nicht das ganze Genom. "Die Rohdaten würden wir löschen", sagt die Professorin für Translationale Medizinethik, die auch Mitglied im Deutschen Ethikrat ist. Entscheidend für die Akzeptanz eines solchen Screenings sei auch eine fundierte Beratung der Eltern, am besten noch während der Schwangerschaft, etwa durch die Gynäkologen.
Wichtig wäre der Wissenschaftlerin bei einem flächendeckenden Angebot des Genomischen Neugeborenen-Screenings auch, dass es für alle bezahlbar bliebe - etwa durch eine Kostenübernahme durch die Kassen. Aktuell erhalten Kliniken für ein klassisches Neugeborenen-Screening knapp 45 Euro erstattet, wie Schaaf sagt. Demnach liegen die reinen Sachkosten für die Sequenzierung eines Genoms aktuell noch bei etwa 1.200 Euro. Allerdings sinken die Preise seit Jahren.
Ein Genomisches Neugeborenen-Screening ist laut Ralf Müller-Terpitz von der Universität Mannheim rechtlich bereits heute möglich - zumindest unter Berücksichtigung gewisser Auflagen. So schreibe etwa das Gendiagnostikgesetz vor, dass die Aufklärung der Eltern zu einem solchen Screening nur durch Ärzte erfolgen dürfe, sagt der Rechtswissenschaftler.
Mutter fordert Aufnahme der Krankheit der Tochter in das Screening
Verena Romero aus Hofheim am Taunus bei Frankfurt kämpft seit Jahren für eine Aufnahme der seltenen genetischen Erkrankung dup15q in das Neugeborenen-Screening - auch wenn sich die Erkrankung nicht behandeln lässt. Bei ihrer Tochter Chiara wurde im Alter von 15 Monaten die Diagnose gestellt, wie Romero erzählt. Da hatte die Familie schon eine monatelange Odyssee von Arzt zu Arzt hinter sich - und die Tochter Tausende von Anfällen, zunächst gab es den Verdacht auf Epilepsie. Das Kleinkind verlernte alles. Es sei zurückgefallen auf den Stand von einem ein oder zwei Monate alten Baby, sagt Romero. Nach der Diagnose erhält Chiara ein anderes Medikament, das die Anfälle erst einmal stoppt.
Romero will anderen betroffenen Familien eine möglicherweise jahrelange Ungewissheit bis zur Diagnose ersparen. Die Symptome ließen sich auch mit der Diagnose besser behandeln, sagt sie. Und: Eine Aufnahme in das Neugeborenen-Screening schaffe die Möglichkeit, sich frühzeitig mit anderen Betroffenen auszutauschen und sich gegenseitig zu unterstützen. "Es ist für uns extrem wichtig, dass man dieses Auffangnetz hat, weil das Versorgungssystem das einfach nicht abdecken kann."

© Uwe Anspach/dpa
Christian Schaaf vom Universitätsklinikum Heidelberg forscht zum Genomischen Neugeborenen-Screening.

© Uwe Anspach/dpa
Am Universitätsklinikum Heidelberg wird für Babys das Neugeborenen-Screening angeboten - und zum Genomischen Neugeborenen-Screening geforscht.
© picture alliance / Stefan Sauer/dpa-Zentralbild/dpa
Ein Bluttropfen vom Fuß eines Babys genügt, um viele Krankheit zu erkennen. (Archivbild)
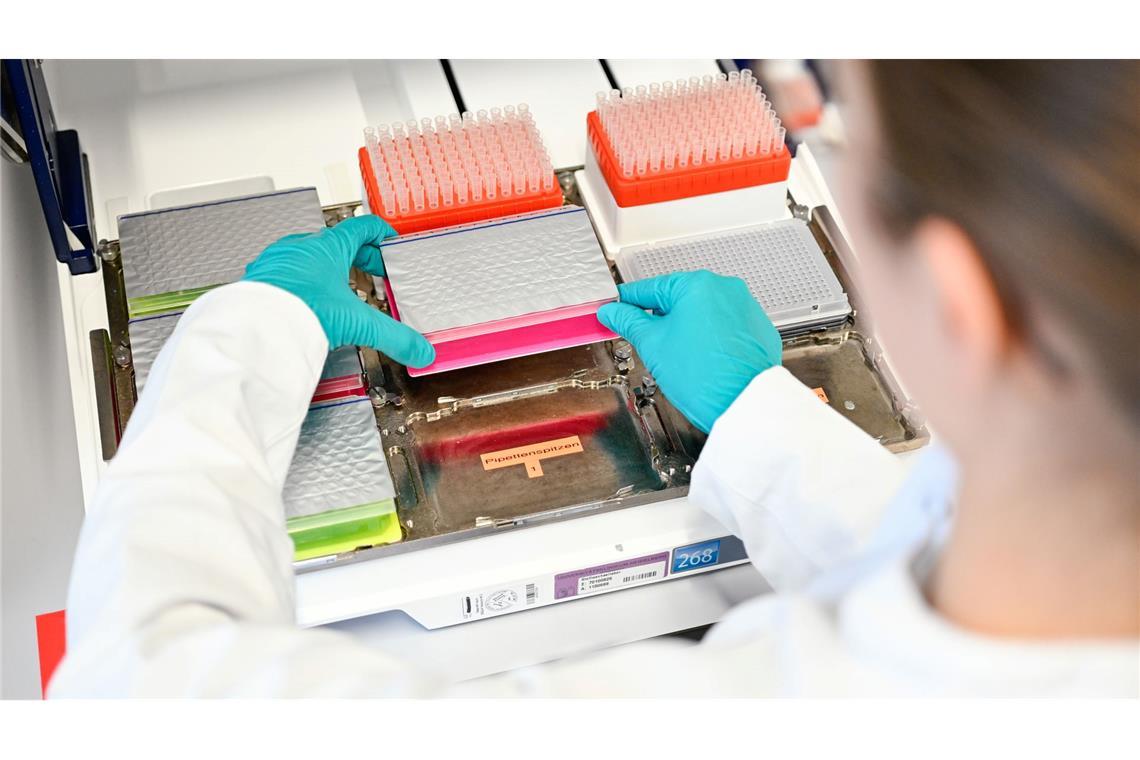
© Uwe Anspach/dpa
Am Universitätsklinikum Heidelberg wird für Babys das Neugeborenen-Screening angeboten - und zum Genomischen Neugeborenen-Screening geforscht.

© Uwe Anspach/dpa
Eva Winkler, Geschäftsführende Direktorin des Nationalen Centrums für Tumorerkrankungen (NCT), ist die Sprecherin des Forschungsverbundes für das Projekt New Lives zum Genomischen Neugeborenen-Screening.



